Uromastyx
Fiche d'élevage des Uromastyx par Olivier ANTONINI
Tableau 1. Classification du genre Uromastyx MERREM 1820
COMPLEXE DES "ACANTHINURA"
1. Uromastyx acanthinura acanthinura BELL 1825 est de l’Algérie, sud de laTunisie, nord–ouest de la Lybie
Uromastyx acanthinura nigriventris ROTHSCHILD & HARTERT 1912 nord et sud-ouest de l’Algérie, Maroc
2. Uromastyx dispar dispar HEYDEN 1827 Soudan, Tchad
Uromastyx dispar flavifasciata MERTENS 1962 Sahara Occidental, Mauritanie, sud–ouest de l’Algérie
Uromastyx dispar maliensis JOGER & LAMBERT 1996 nord–est du Mali, sud-ouest de l’Algérie
3. Uromastyx geyri MÜLLER 1922 sud de l’Algérie, nord–est du Mali, nord–ouest du Niger (Hoggar)
4. Uromastyx alfredschmidti WILMS & BÖHME 2000 ouest de la Lybie, sud–est de l’Algérie
COMPLEXE DES "AEGYPTIA"
5. Uromastyx aegyptia aegyptia (FORSKALL 1775) Egypte (à l’est du Nil), Soudan, Israël
Uromastyx aegyptia microlepis BLANFORD 1874 nord de l’Arabie Saoudite, Israël, Syrie, Irak, Iran, Jordanie
6. Uromastyx leptieni WILMS & BÖHME 2000 nord d’Oman, est des Emirats Arabes Unis
7. Uromastyx occidentalis MATEO et al. 1999 Sahara Occidental
UROMASTYX D’IRAN
8. Uromastyx asmussi (STRAUCH 1863) nord et est d’Iran, sud–ouest d’Afghanistan, sud– ouest du Pakistan
UROMASTYX INDIEN
9. Uromastyx hardwickii GRAY 1827 Pakistan, sud-est de l’Afghanistan, nord de l’Inde
UROMASTYX D’IRAK
10. Uromastyx loricata (BLANFORD 1874) centre–nord d’Irak, sud–ouest d’Iran
COMPLEXE DES "OCELLATA"
11. Uromastyx benti (ANDERSON 1894) Yemen, Oman, sud de l’Arabie Saoudite
12. Uromastyx ocellata LICHTENSTEIN 1823 nord-ouest de la Somalie, Djibouti, Erythrée,
nord du Soudan, sud–est de l’Egypte
13. Uromastyx ornata ornata HEYDEN 1827 est de l’Egypte, sud d’Israël, nord–ouest de l’Arabie Saoudite
Uromastyx ornata philibyi PARKER 1938 Arabie Saoudite, Yemen
14. Uromastyx macfadyeni PARKER 1932 nord-ouest de la Somalie
UROMASTYX DE SOMALIE
15. Uromastyx princeps O’ SHAUGHNESSY 1880 Somalie
UROMASTYX D’OMAN
16. Uromastyx thomasi PARKER 1930 Oman
Le genre Uromastyx MERREM, 1820 fait partie de la famille des Agamidae.
Selon la nouvelle classification proposée par WILMS et BÖHME en 2001, il comprend 16 espèces et 9 sous-espèces (Tableau 1).
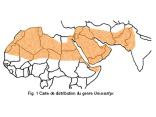
La zone de répartition du genre Uromastyx est une zone très étendue qui, à partir du Sahara occidental, traverse tout le Nord de l’Afrique, le Moyen Orient, l’Irak, l’Iran, le Sud de l’Afghanistan, le Pakistan jusqu’au Nord-Ouest de l’Inde (Fig. 1).
Uromastyx, appelé « dob » en arabe et « fouette-queue » en français en raison de la manière de se défendre en fouettant avec sa queue épineuse, est un lézard herbivore, terrestre, sédentaire, diurne et héliophile. Il occupe les biotopes pierreux et rocheux des milieux désertiques et semi–désertiques tandis qu’on ne le trouve pas sur les étendues sablonneuses (dunes) qui constituent des barrières à ses déplacements.
Toutes les espèces d’Uromastyx sont classées en ANNEXE II de la Convention internationale sur les espèces en danger (Convention on International Trade in Endangered Species, C.I.T.E.S.) dite aussi "Convention de Washington". Les individus prélevés dans la nature doivent être donc vendus avec un numéro de CITES. Ceci permet de contrôler le commerce international de cette espèce qui est considérée comme relativement menacée dans son habitat naturel.
L’importation des Uromastyx en Europe occidentale est limitée seulement à certaines espèces qui sont donc plus connues que d’autres par leur détention et reproduction en captivité.
A ma connaissance, on peut se procurer, en France, à ce jour, Uromastyx acanthinura nigriventris, Uromastyx dispar maliensis, Uromastyx dispar flavifasciata, Uromastyx geyri, Uromastyx aegyptia aegyptia, Uromastyx ocellata, Uromastyx ornata ornata et Uromastyx hardwickii.
Les notes qui suivent concernent la maintenance de huit espèces et sous–espèces d’Uromastyx :
– Uromastyx acanthinura nigriventris
– Uromastyx dispar maliensis
– Uromastyx dispar flavifasciata
– Uromastyx geyri
– Uromastyx aegyptia aegyptia
– Uromastyx ocellata
– Uromastyx ornata ornata
– Uromastyx hardwickii
Parmi ces espèces et sous–espèces, quatre ont été reproduites entre 2000 et 2003 dans les locaux de l’association Bébésaurus, c’est-à-dire : U. a. nigriventris, U. d. maliensis, U. geyri et U. ocellata.
Aménagement du terrarium
Les dimensions du terrarium varient selon la taille et l’âge des animaux.
Les couples reproducteurs de taille moyenne (U. acanthinura, U. d. maliensis, 35-40 cm environ) ainsi que les petits groupes (3 ou 4 individus) d’Uromastyx de petite taille (U. ocellata, 30 cm maximum) ou de taille moyenne (U. o. ornata, U. geyri, 35 cm environ) sont logés dans des terrariums qui ont une surface au sol de 100 x 100 cm ou 180 x 50 cm.
Les deux groupes de 3 individus U. a. aegyptia, Uromastyx de grande taille (70-75 cm maximum) sont logés dans des terrariums de 200 x 100 cm.
Un groupe de 8 individus U. hardwickii (35 cm environ) est logé dans un terrarium de 200 x 100 cm.
Les juvéniles (20-25 cm) sont logés seuls dans des terrariums 100 x 50 cm.
Quand cela est possible, une bonne profondeur sera privilégiée car Uromastyx se sent plus en sécurité s’il a du recul par rapport à l’"extérieur".
La hauteur des terrariums varie entre 50 cm et 60 cm. Ceci permet d’aménager, grâce au décor (souche, écorce de liège…), un endroit près du tube néon (30 cm maximum), là où les lézards peuvent profiter du rayonnement UVA et UVB. Généralement, Uromastyx ne grimpe pas sur les branches, sauf U. ocellata et U. o. ornata, ou les juvéniles.
Sur les côtés du terrarium ou au plafond il y a des aérations grillagées (mes terrariums sont en bois sur les trois côtés, avec des vitres sur glissières devant) qui permettent un changement d’air suffisant et empêchent la surchauffe du terrarium.
Sur un côté du terrarium je mets un spot de 60W (ou une lampe à vapeur de mercure mixte de 160W pour les terrariums 200 x 100 cm) à 20 cm du sol et avec une pierre plate au-dessous de manière à créer un point chaud qui atteint 45 à 50° C. Au point le plus frais, au côté opposé, la température sera de 28° C environ. Un bon gradient thermique est très important car il permet à l’animal de régler sa température interne par des adaptations comportementales. Ainsi qu’il le fait dans le milieu naturel, Uromastyx se chauffe, le matin, par rayonnement en se dressant sur les pattes antérieures, le dos vers la source de chaleur. Cependant, en captivité on peut souvent observer l’animal se chauffer aussi par conduction en s’aplatissant sur la pierre situé sous le spot. Quand il a atteint sa température optimale il s’éloigne de lui-même vers le point le plus frais du terrarium. S’il n’arrive pas à baisser suffisamment sa température interne [c’est-à-dire si celle–ci reste supérieure à 39° C en milieu naturel (Grenot, 1976)], Uromastyx manifestera son état par une ventilation rapide en ouvrant la bouche (polypnée thermique), ce qui représente un moyen de refroidissement par évaporation bucco-pharyngée (Grenot & Loirat, 1973).
Selon la saison et la température de la pièce, je mets en place un tapis chauffant (Habistat®) qui, à la différence des câbles chauffants, ne peut pas être aisément déterré.
Une forte luminosité et une chaleur importante sont essentiels pour une maintenance correcte d’Uromastyx en captivité. Ces données sont maintenues constantes pendant la durée du jour qui sera de 14 heures au maximum en août et de 8 heures au minimum pendant la période d’hivernage (voir chapitre sur la reproduction).
Les juvéniles sont chauffés par un petit spot de 40W : leur besoin de chaleur est sensiblement le même que celui des adultes.
La nuit le chauffage est coupé et la température du terrarium redescend à la température de la pièce qui varie, selon les saisons, entre 15 et 30° C.
En ce qui concerne le substrat, après avoir presque tout essayé et avoir aussi perdu un individu par occlusion intestinale causée par un éclat de hêtre, j’ai opté pour le Litalabo®, ce sont des minuscules copeaux de bois conçus pour les cobayes qui, même s’ils sont ingérés, ne provoquent pas des blessures internes car ils ne sont pas coupant et sont éliminés avec les excréments. Une idée intéressante nous vient des Etats Unis où certains éleveurs maintiennent leurs Uromastyx sur un substrat constitué de graines pour oiseaux; en ce qui me concerne, je trouve un tel aménagement pas vraiment économique ni hygiénique.
Les nouveau-nés et les juvéniles jusqu’à 11cm environ sont maintenus sans substrat ou sur du Sopalin, ce qui me permet de contrôler plus facilement leurs excréments, source de renseignements sur leur état de santé. Pour la même raison, je garde sans substrat les animaux malades.
Le décor de mes terrariums est constitué en premier lieu d’une écorce (ou une tuile), indispensable pour le bien-être de ces lézards qui s’y cachent quand ils sont stressés ou quand ils dorment. Cet abri est placé du côté frais du terrarium. Pour qu’ils s’y sentent en sécurité, quand ils y sont debout la tête doit toucher le "plafond" ou, mieux encore, ils ne doivent pas pouvoir s’y tenir debout. En principe, il doit y avoir une cachette par animal, mais j’ai constaté que souvent ils dorment dans la même sans problèmes.
Une souche assez grande pour permettre aux animaux de s’approcher du tube néon installé au plafond et qui peut être escaladée facilement –ou une écorce qui monte vers le néon– constitue la dernière pièce indispensable du décor. Selon la place à disposition, j’ajoute également des cactus en plastique, des cailloux, parfois des branches, en prenant toutefois garde à qu’il y ait toujours un espace ouvert suffisant pour permettre aux lézards de se déplacer aisément et notamment de s’accoupler.
Etant donné la puissance que ces lézards ont dans leur mâchoire et la capacité coupante de leurs dents, j’évite les plantes en plastique, dont les feuilles peuvent être ingérées, ainsi que n’importe quelle plante véritable. Je fais aussi attention à que les éléments du décor ne soient pas simplement appuyés sur le substrat mais qu’ils touchent le fond du terrarium car, en creusant, les fouette–queues risquent de se faire écraser par la souche, les pierres etc. (en particulier les juvéniles et les animaux de petite taille).
Tous les deux mois je change le substrat et je passe tout, y compris le décor, à l’eau de javel.
Alimentation en captivité
Uromastyx est un lézard herbivore. En milieu désertique, le fouette–queue ne s’alimente pas de manière régulière mais en suivant le cycle des saisons selon les précipitations, plus au printemps, peu en été, de nouveau en automne, presque pas en hiver (Grenot, 1976). En captivité également il est indispensable de suivre un cycle annuel dans la prise de nourriture, qui sera plus fréquente et plus riche au printemps et en automne, plus espacée en été et inexistante pendant l’hivernage.
En terrarium, son menu de base comprend en premier lieu des végétaux, notamment des feuilles, des salades et des légumes. Les salades et les feuilles que je leur donne sont de préférence celles qui ont un bon rapport phospho-calcique (deux fois plus de calcium que de phosphore), donc scarole, mâche, chicorée, cresson, frisée, romaine, endives, blettes, pissenlit, trèfle, luzerne, fanes de carottes, de navets et de radis, faux acacia (robinier), mûrier–platane, lierre terrestre (Glechoma hederacea), grand plantain (Plantago major), Malva silvestris.
Les fleurs aussi constituent un mets de choix, par exemple les fleurs de pissenlit, trèfle, robinier, courgette, hibiscus, forsythia, genêt, pâquerette, robinier, luzerne, mimosas.
Avec une fréquence hebdomadaire variable selon la saison (à titre indicatif : trois fois par semaine au printemps, une fois par semaine en été, deux fois par semaine en automne) je leur donne également un parmi ces légumes : haricots verts, petits pois, courgettes (vendus congelés en sachets et préalablement décongelés), carottes crues râpées ou partiellement cuites, choux de Bruxelles, lentilles (réhydratées), pois chiches (réhydratés), pois cassés (réhydratés), haricots mungo (réhydratés).
Pour ce qui concerne les fruits, je dois dire que mes Uromastyx ne les aiment pas, sauf peut-être les figues et les figues de barbarie. Mais c’est vrai aussi que les goûts changent d’un individu à l’autre et que leurs préférences changent avec le temps. D’ailleurs, n’importe quelle nourriture peut être refusée aujourd’hui et appréciée demain.
Régulièrement, deux fois par mois environ, je leur prépare une coupelle de graines (30 gr environ) que je mélange avec du carbonate de calcium. A la différence des salades et des légumes que je donne indifféremment aux adultes et aux juvéniles (ce qui change est évidemment la taille des "morceaux"), les graines ne sont pas les mêmes selon l’âge de l’animal. Pour les juvéniles (à partir de 12 cm de longueur totale) : lin doré et brun, quinoa, millet, alfalfa (c’est-à-dire graines de luzerne), tandis que le sarrasin est distribué aux jeunes de plus de 20 cm. Pour les adultes : blé, orge décortiqué, sarrasin, tournesol, cacahouètes non grillées pour perroquets, ainsi que les graines des juvéniles. Aux bébés je ne donne pas de graines par crainte d’occlusion intestinale.
Etant donné le comportement des mes Uromastyx, ces graines ont vite fait de se retrouver éparpillées partout et mélangées au substrat : ça leur permet de se constituer une "réserve" de nourriture, avec des morceaux de légumes ou de salade séchés, que les fouette–queues déterrent par des mouvements vifs des pattes. En fait, même si j’enlève tous les jours le plus gros de la nourriture non consommée, on ne peut empêcher que des débris de ces aliments restent mélangés aux copeaux : mais l’environnement sec dans lequel je les maintiens évite qu’ils pourrissent et ils peuvent donc être consommés (d’ailleurs j’ai remarqué que parfois les Uromastyx les préfèrent aux aliments frais).
La salade et les légumes sont saupoudrés avec du carbonate de calcium trois fois par semaine (tous les jours pour les juvéniles et les femelles en phase de reproduction), tandis qu’une fois par semaine (deux pour les jeunes) j’ajoute à la nourriture des vitamines avec un mélange de "Petphos® croissance" (complément vitaminique pour chiots) et de vitamines pour oiseaux (Ocevital®).
En ce qui concerne les insectes, Uromastyx en captivité mange volontiers grillons, criquets, morios ou vers de farine, mais cette nourriture n’est pas indispensable pour sa bonne santé, en particulier si on lui donne des protéines végétales (par exemple avec les petits pois ou les haricots verts); il y a même des éleveurs étasuniens qui ont maintenu leurs Uromastyx, adultes et juvéniles, pendant des années sans leur donner aucun insecte. De plus, chez les adultes, une nourriture trop riche en protéines animales risque de provoquer des maladies hépatiques qui peuvent causer la mort du lézard végétarien, un risque moins important pour les juvéniles ou les femelles en période de reproduction. La distribution des insectes sera donc occasionnelle, plus fréquente pour les femelles gravides ou qui viennent de pondre et pour les juvéniles. Des insectes toujours saupoudrés de carbonate de calcium et de vitamines et bien nourris par mes soins. En sachant toutefois que certains des mes Uromastyx ne les apprécient guère, notamment les U. aegyptia aegyptia, tandis que les U. ocellata et U. hardwickii en raffolent. Je me suis aussi "appuyé" sur les insectes pour démarrer les nouveau-nés, petits grillons et vers buffalos : apparemment, le mouvement des proies excite les bébés.
Compte tenu de son aire de distribution, Uromastyx ne boit presque jamais d’eau libre en milieu naturel. En captivité, j’ai remarqué que seulement les femelles gravides ou ayant récemment pondu, les nouveau-nés, les animaux fraîchement importés ou malades buvaient systématiquement. Dans ces cas je leur mets à disposition une coupelle plate d’eau. Certains éleveurs préconisent une légère vaporisation matinale dans un coin du terrarium (Wilms, 2002) : pour ce qui me concerne, je ne le fais pas en craignant que cela puisse entraîner une hygrométrie trop importante dans le terrarium.
Comportement en captivité
Le comportement d’Uromastyx en captivité varie d’un individu à l’autre et, surtout, s’il s’agit d’un animal né en captivité ou sauvage, déjà acclimaté ou de récente acquisition, bien nourri et bien chauffé ou stressé et malade. Mais, en règle générale, à partir de mon expérience, je pense que l’idée qu’il s’agit d’un lézard farouche, qui passe sa journée caché, qui essaye de mordre dès qu’on le touche et que de toute façon on ne peut pas manipuler, est fausse. Ce que j’ai constaté c’est qu’au contraire Uromastyx, surtout s’il est né en captivité, est un lézard très curieux qui regarde avec intérêt tout ce qui se passe autour de lui, en général il peut être manipulé sans que cela provoque un état de stress tandis qu’il faut éviter de le contenir, la contrainte étant mal supportée par l’animal.
Une fois dépassée la crainte de l’homme –crainte qui, quand elle existe, influence négativement le comportement du lézard– Uromastyx est un sujet idéal d’observation. Ceci est encore plus vrai si on maintient un couple ou un groupe car le comportement interspécifique est très varié selon la saison, et particulièrement intéressant à la saison des accouplements.
D’une manière générale, parmi les espèces d’Uromastyx que je possède, U. acanthinura et U. dispar maliensis peuvent être maintenus en couple. Sur la base de mon expérience, j’ai remarqué qu’il existe une incompatibilité entre mâles ainsi qu’entre femelles de ces espèces. En fait, non seulement les mâles se "bagarrent" mais les femelles aussi peuvent être agressives entre elles, notamment avant et après la ponte. Les morsures ne sont pas mortelles en soi, c’est-à-dire qu’en générale ils ne s’arrachent pas des morceaux de chair, ne s’étripent pas, souvent ils ne saignent même pas. Pour ce que j’ai pu constater, deux cas de figure peuvent se présenter : ou les deux "bagarreurs" se tiennent tête ou un des deux s’avoue vaincu et s’échappe sous la cachette la plus proche.
Dans le premier cas, ils se font face en élargissant et aplatissant leur corps, ils tournent en rond "en biais" en montrant ainsi le dos large et rond et ils se mordent mutuellement sur les côtés ou aux cuisses, à l’épaule, à la queue, et, en gardant fortement prise, ils essayent de renverser l’adversaire. Ce qui veut dire que non seulement ils se pincent avec leur "bec" puissant mais la peau pincée est "vrillée" avec des brusques mouvement de tête. Ces batailles peuvent durer longtemps, jusqu’à ce qu’un parmi les adversaires s’enfuie, et même si les blessures ne paraissent pas graves sur le coup, par la suite sous la peau meurtrie se développent des abcès qu’il faut s’empresser de soigner pour empêcher qu’ils évoluent en septicémie (favorisée par l’état de stress profond qui suit l’affrontement). Finalement, là où la peau a été meurtrie les écailles ne repoussent pas et pendant longtemps il reste une peau lisse et blanche.
Dans le deuxième cas de figure, le plus faible ne se bat pas mais il n’a pas de répit non plus, contraint à rester caché il se nourrit peu et mal, ne se chauffe pas et le stress continu dans lequel il vit affaiblit son organisme en ouvrant la voie à diverses maladies.
Au contraire, les couples vivent ensemble sans trop se disputer, je les sépare seulement une semaine avant la ponte pour permettre à la femelle de pondre tranquillement et éviter d'éventuels dommages aux œufs. Les seuls problèmes que j’ai constaté concernent éventuellement l’insistance avec laquelle le mâle essaye de s’accoupler : si la femelle n’est pas réceptive elle peut "stresser" au point de ne plus vouloir sortir de son repaire. C’est à l’éleveur d’évaluer si le mâle peut rester dans le terrarium ou s’il doit être momentanément isolé.
Parmi les autres espèces, U. ocellata peut (sauf exceptions) être maintenu "en harem", un mâle avec deux ou trois femelles. Il arrive de temps en temps que les femelles montrent une certaine agressivité entre elles mais il s’agit d’escarmouches pas vraiment sérieuses. Bien évidement l’éleveur devra toujours rester vigilant pour déceler tout changement dans le comportement qui pourrait entraîner des combats dangereux pour les animaux.
U. a. aegyptia également est maintenu "en harem", un mâle pour deux femelles. Cependant, quand une des deux femelles a atteint la maturité sexuelle et s’est accouplée, elle est devenue de plus en plus agressive à l’approche de la date de ponte, au point que j’ai été contraint d’enlever le mâle et l’autre femelle. Après la ponte et jusqu’à aujourd’hui (deux mois après la ponte) ça n’a pas été possible de reconstituer le groupe, la femelle qui a pondu attaque systématiquement les deux autres individus.
Pour ce qui concerne U. hardwickii, je maintien depuis presque deux ans huit individus ensemble, quatre adultes (un mâle et trois femelles) et quatre sub–adultes (un mâle et trois femelles) et je n’ai observé aucune manifestation d’agressivité. Dans le milieu naturel, U. hardwickii a tendance à vivre en colonies (Minton, 1966).
Finalement, pour U. geyri j’ai vérifié depuis deux ans que l’on peut maintenir les individus de cette espèce en petits groupes composés de deux ou trois mâles et deux ou trois femelles sans qu’il se manifeste aucune agressivité interspécifique, même pendant la période des accouplements. Même s’il y a toujours une hiérarchie, tous les individus évoluent normalement et ils ne souffrent pas de la cohabitation. J’ai même assisté à un "accouplement à quatre", c’est-à-dire que dès qu’un jeune mâle a commencé à s’accoupler avec une femelle, le plus gros mâle, plus vieux, est arrivé pour prendre sa place et tout de suite après un deuxième jeune mâle a aussi tenté sa chance de manière que pendant quelques minutes la femelle avait trois mâles accrochés sur son dos ! En définitive c’est le plus gros qui a fini pour s’accoupler. Chez un autre groupe, les deux femelles se sont accouplées à tour de rôle avec les deux mâles.
Pour ce qui concerne les juvéniles, quand ils sont maintenus en groupe, ils suivent souvent les mêmes schémas des adultes. Les jeunes U. acanthinura et U. dispar maliensis peuvent parfois cohabiter dans le même terrarium pendant un laps de temps mais il s’agit toujours d’un équilibre instable vite rompu par l’individu qui, en assumant le rôle de dominant, poursuit d’un bout à l’autre du terrarium ses frères et sœurs en leur mordant les flancs et la queue. Ainsi il ne donne plus de répit aux autres en leur "volant" la meilleure place au "soleil" la plus belle cachette, souvent en les empêchant de s’approcher de la nourriture. La condition d’individu dominé est dangereuse à plus forte raison pour un jeune animal et ne peut être maintenue longtemps. C’est pourquoi je garde séparés les juvéniles dès qu’ils deviennent agressifs entre eux : j’ai essayé d’éloigner le dominant mais en l’espace de quelques jours un autre dominant s’impose et le "cirque" recommence.
Au contraire, les juvéniles U. ocellata, U. a. aegyptia, U. hardwickii et U. geyri ont grandi ensemble sans problèmes.
REPRODUCTION EN CAPTIVITÉ
Tout d’abord je veux préciser que mon expérience dans la reproduction des Uromastyx est très limitée : j’ai reproduit Uromastyx ocellata en 2000, 2002, 2003 et 2004, Uromastyx acanthinura et Uromastyx dispar maliensis en 2001, 2002, 2003 et 2004, Uromastyx geyri en 2002, 2003 et 2004, Uromastyx a. aegyptia en 2004 et U. hardwickii en 2004. Toutefois, même si, d’après moi, pour une bonne maîtrise de la reproduction sont nécessaires plusieurs années consécutives de succès, je pense avoir appris quelques éléments de base qui ont été jusque là confirmés par des résultats positifs.
hivernage
La première et la deuxième année que j’ai reproduit mes Uromastyx, je n’ai pas entamé un véritable processus d’hivernage. N’ayant pas connaissance de donnés sur ce sujet et en me fondant sur l’idée, fausse, que la reproduction des Uromastyx en captivité est très difficile voir impossible, j’ai laissé vivre mes animaux en hiver dans les mêmes conditions que le reste de l’année hormis une baisse de photopériode (10 heures en hiver, 14 heures en été). Du moins c’est ce que je croyais…. J’ai été donc très surpris quand, le 27/02/2000 j’ai vu mes Uromastyx ocellata s’accoupler. Avec le recul, en cherchant les raisons de cet exploit, je me suis rendu compte que le câble chauffant ne marchait plus depuis au moins un mois et que donc dans le terrarium il y avait eu une baisse, ni voulue ni maîtrisée, de la température. Un scénario similaire s’est produit l’année suivante pour une partie des mes Uromastyx acanthinura et Uromastyx dispar maliensis, justement ceux qui se sont reproduit en 2001, tandis que d’autres femelles de la même espèce logées dans un autre terrarium où la température est restée élevée tout le long de l’hiver, ne se sont pas accouplées.
Fort de cette expérience, et en ayant entre temps pris connaissance des procédés employées
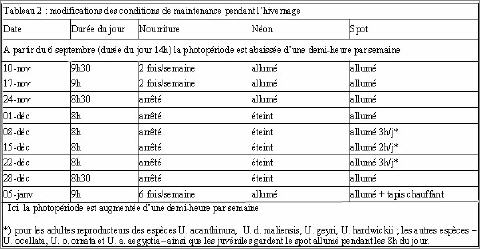
par des éleveurs étasuniens dans la reproduction d’Uromastyx, j’ai mis au point un schéma d’hivernage (voir Tableau 2) qui a été appliqué notamment aux adultes Uromastyx acanthinura, Uromastyx dispar maliensis et Uromastyx geyri.
Pendant les trois semaines "critiques" du 08-déc au 28-déc j’ai multiplié mes observations pour m’assurer que tout se passait bien et j’ai remarqué qu’en moyenne un jour sur trois les fouette–queues sortaient de leur cachette pour se chauffer sous le spot en se retirant dès que les trois (ou deux) heures étaient écoulées. Un tel procédé (et aussi parce-que la température ne descendait jamais au-dessus de 15° C, température minimale atteinte la nuit) permet au lézard de garder sa température interne à l’intérieur des limites vitales.
En revanche, les adultes Uromastyx ocellata, Uromastyx o. ornata, Uromastyx a. aegyptia et Uromastyx hardwickii continuent pendant toute la durée de l’hivernage à bénéficier de la chaleur et de la lumière diffusées par les spots pendant les 8 heures du jour, mais la luminosité diminue car le néon est éteint et les animaux ne se nourrissent pas. Cette différence de traitement est due au fait que ces espèces subissent à l’état sauvage un hivernage plus doux que les autres espèces du Sahara. Pour ces espèces (ainsi que pour U. benti) une baisse de température de 5°-10° C en hiver serait suffisante pour stimuler le cycle reproducteur (T. Wilms, 2001).
A ce propos, il faut se rattacher aux observations de C. Grenot (1976) en milieu naturel : la température, la lumière et l’humidité influent directement sur le cycle sexuel mais ce serait l’augmentation progressive de la photopériode le stimulus principal qui détermine le début de l’activité sexuelle. L’abondance en végétaux qui suit les pluies printanières aurait aussi un rôle important dans ce processus.
Les juvéniles de ces mêmes espèces bénéficient également d’un changement saisonnier, c’est–à–dire la journée de 8 heures ainsi qu’une relative baisse de température notamment la nuit ; en revanche, le néon et le spot restent allumés pendant les 8 heures du jour. La nourriture leur est proposée deux à trois fois par semaine.
Si une période de repos hivernale est nécessaire pour reproduire le genre Uromastyx, je crois qu’un léger hivernage est bénéfique à tout âge et indépendamment de l’objectif de la reproduction, il permet de marquer le mouvement des saisons et, peut-être, contribue à reproduire un environnement plus naturel donc plus favorable au bien-être des animaux en captivité.
Accouplement
Les parades d’accouplement menées par les mâles se heurtent souvent, au début, à un net refus de la part des femelles. Le mâle commence par des amples hochements de tête verticaux qui entraînent aussi les pattes antérieures en donnant l’impression qu’il "fait des pompes". En même temps il tourne frénétiquement autours de lui-même et au-dessus de la femelle et il essaye de la mordre sur les côtés, sur le dos, à la nuque. Si elle n’est pas réceptive, la femelle essaye de s’échapper, une fois attrapée agite fortement les pattes et, pour être encore plus claire dans son refus, se met sur le dos, ventre en l’air. Cette position rend impossible l’accouplement et le mâle, après avoir valsé en rond inutilement sur le ventre de la femelle, la laisse tranquille pour essayer de nouveau plus tard.
Quand la femelle est réceptive elle ne s’enfuit pas face aux avances du mâle et, quand il la pince au cou ou sur le dos, elle soulève la queue en favorisant ainsi la pénétration d’un des deux hemipenis du mâle. L’accouplement dure 3–5 minutes, il peut y en avoir plusieurs le même jours (même avec des mâles différents) et, à ma connaissance, les Uromastyx s’accouplent pendant environ une semaine, jusqu’à 11 jours, tous les jours.
Gestation
D’une manière générale, la ponte a lieu entre 4 à 6 semaines à compter du dernier jour d’accouplement (Tableaux 3 a, b, c, d).
Ponte
Mes Uromastyx pondent une seule fois par an. Cependant, d’après certains auteurs (Doumergue, 1901 ; Bons, 1969 ; Wilms, 2001) il pourrait y avoir deux pontes par an, séparées par une petite période de repos pendant l’été chez U. acanthinura.
Une semaine environ avant la ponte, la femelle s’arrête de manger et elle commence à creuser un peu partout, de manière de plus en plus acharnée à mesure que la date de la ponte approche. Des renflements abdominaux peuvent parfois trahir la présence des œufs, mais pas nécessairement. A ce moment là, je place dans le terrarium une boite de ponte. Il s’agit d’une bassine 30 x 40 x 15 cm environ remplie de vermiculite légèrement humide ; sur le devant de cette bassine j’ai pratiqué une ouverture ronde de 8 ou 10 cm de diamètre dans laquelle j’ai inséré un tuyau flexible (tuyau de VMC) long de 40 à 50 cm qui représente le "tunnel" d’accès à la "chambre de ponte". Cette dernière est ensuite fermée avec une plaque en PVC.
D’une manière générale, la femelle accepte cette chambre de ponte si le "plafond" est suffisamment bas, c’est–à–dire si elle ne peut pas s’y tenir debout ; pour la sécuriser encore plus j’enlève le mâle qui a la fâcheuse tendance de "squatter" ce pseudo-terrier. Si elle refuse d’y pondre, je vérifie la température (qui ne doit pas être plus élevée au fond de la boite par rapport à le surface) et l’hygrométrie (la vermiculite doit être légèrement humide).
Une fois la ponte effectuée, je retire les œufs et je les place dans l’incubateur. Parfois, la femelle continue pendant une à deux semaine à "protéger" son site de ponte en empêchant le mâle de s’y approcher, en soufflant et en le poursuivant jusqu’aux frontières de son territoire.
Le nombre des œufs pondus varie selon l’espèce, l’âge et la taille (Tableau 3 a, b, c, d).
Incubation
Les œufs sont placés dans une boite avec un couvercle troué et remplie de tourbe sèche ; cette boite est ensuite placée dans un incubateur où la température est de 31-32° C et l’humidité de 100% environ. Ces données sont maintenues constantes pendant la durée de l’incubation, en moyenne entre 80 et 90 jours (Tableau 3 a, b, c, d).
L’incubateur dont je me sers est du genre "fait–maison" : un vieux frigo débranché et équipé d’un câble chauffant relié à un thermostat et qui traverse en partie un bac d’eau de la taille du bac à légumes du frigo. Cela me permet d’avoir un environnement isolé, saturé d’humidité et à une température constante : ces données je les retrouve dans les boites car les couvercles sont troués.
D’autres moyens peuvent être envisagés, par exemple certains éleveurs (Wilms, 2001) préfèrent incuber les œufs dans une boite fermée sans aérations et remplie de vermiculite, tout en humidifiant légèrement avec une seringue la vermiculite au fond de la boite, et en ouvrant celle-ci de temps en temps pour permettre le renouvellement de l’air.
Quoiqu’il en soit il est impératif que les œufs ne soient pas posés sur un substrat humide sous peine de les voir moisir. En bref : substrat sec dans un environnement saturé d’humidité.
Quelques jours avant l’éclosion, les œufs peuvent "perler", c’est-à-dire que des gouttelettes se forment sur la surface de la coque. En d’autres cas, les œufs se dégonflent une semaine à dix jours avant l’éclosion ; parfois aucun changement n’est visible.
Naissance
Les naissances sont échelonnées sur 3, 4 jours. Le taux d’éclosion est variable (Tableau 3 a, b, c, d).
Les nouveau-nés U. acanthinura et U. d. maliensis mesurent 8–9 cm environ de longueur totale pour 6 gr environ de poids; les nouveau-nés U. geyri et U. ocellata sont un peu plus petits, 7–8 cm environ de longueur totale pour 3.5–4.5 g environ de poids. Ils sont tout de suite bien vifs et ils commencent à manger deux, trois jours après la naissance.
La croissance est relativement importante les premiers mois. Ensuite, dès que la photopériode diminue, elle ralentit considérablement et elle s’arrête en novembre–décembre. Avec le retour de la "bonne saison" la croissance reprend avec vigueur : à l’âge d’un an, par exemple, les jeunes U. acanthinura mesurent 20 cm environ pour 85 gr de poids, alors que les jeunes U. d. maliensis mesurent 18 cm environ pour 50 gr de poids.
Une mésaventure qui a frappé les premiers mois de vie de mes petits Uromastyx en 2001 est riche en enseignements. Dans un texte d’éleveurs étasuniens j’avais lu qu’ils donnaient à manger à leurs nouveau-nés les excréments des parents : ceci me paraissait sensé car ce genre de "nourriture" favorise la création de la flore intestinale et cette pratique est courante dans la nature chez les animaux végétariens (Iguana iguana, entre autres, mais aussi chez certains marsupiaux comme le koala). Malheureusement, quelques jours après avoir ainsi nourri mes bébés Uromastyx, certains d’entre eux ont commencé à avoir la diarrhée et 10 sont morts avant d’avoir pu être soignés. L’année suivante je n’ai pas répété l’expérience et les jeunes ont grandi normalement. Par contre, le fait que pendant les deux premiers mois de vie les jeunes mangent systématiquement leurs propres excréments ainsi que ceux de leurs frères et sœurs n’a pas d’effets négatifs sur leur santé.
modifications des conditions de maintenance
Lien : http://www.bebesaurus.com